Christophe a écrit :ABC2019 a écrit :d) Ce sont justement les réactions chimiques atmosphériques qui pourraient être impactées (à la baisse) par une "société de l'hydrogène"...
pourquoi ?
C'est un membre ici qui l'a dit il y a quelques jours...
Apparemment l'H2 en haute altitude "attaquerait" les radicaux libres qui permettent justement l'oxydation du méthane...
Il n'avait pas cité la source, quelques recherches s'imposent donc...
C'est moi.
Je ne retrouve plus l'article en question.
Mais:
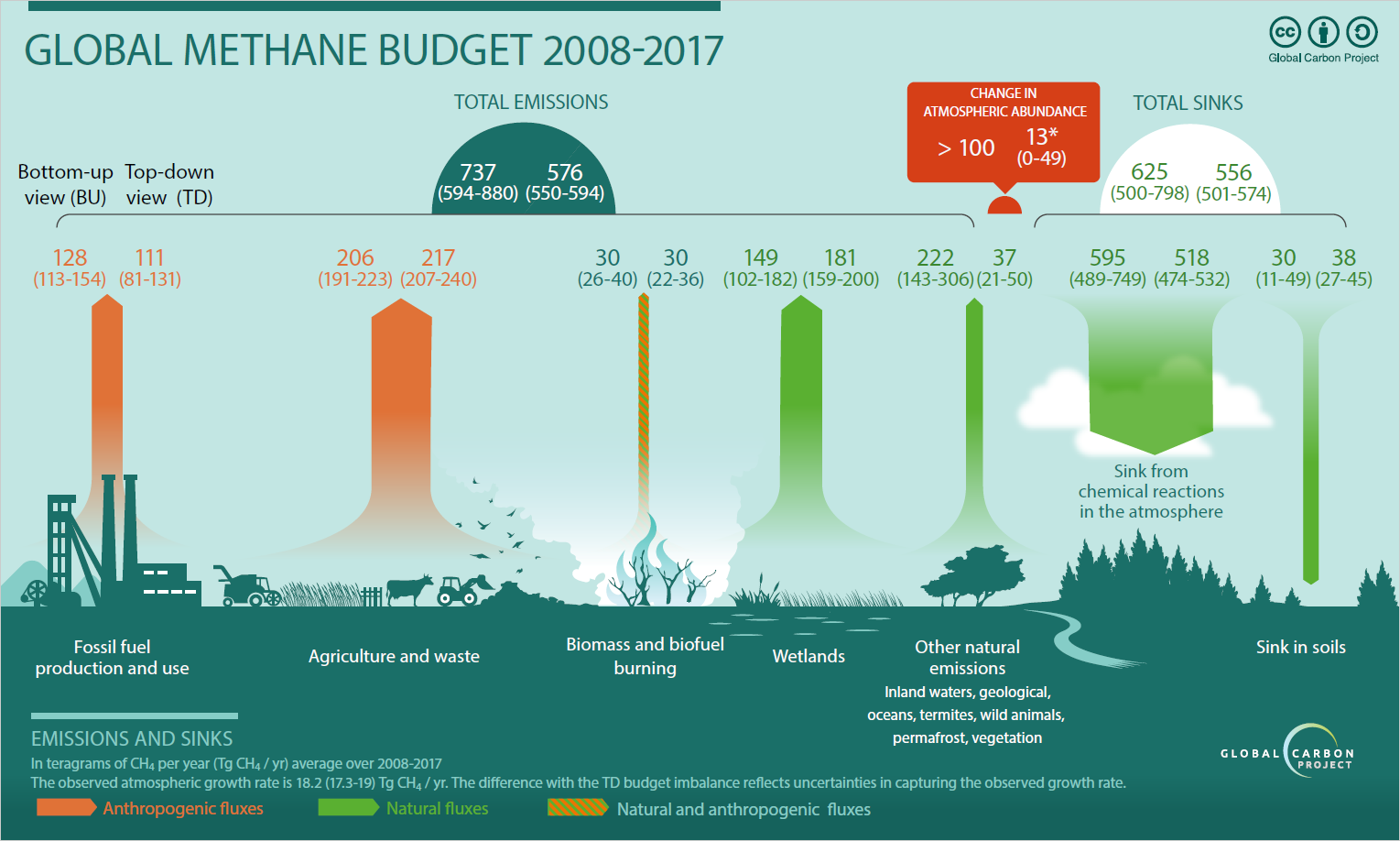
Après émission dans l’atmosphère, le CH4 est oxydé rapidement. La chaîne réactionnelle est complexe, faisant intervenir des radicaux libres hydroxyles (·OH) produits par photolyse de l’ozone en présence de vapeur d’eau (≈ 106 molécules/cm3 d’air dont la durée de vie moyenne est de l’ordre de la seconde). La chaîne réactionnelle principale fait intervenir les oxydes d’azote et produit de l’ozone. En revanche, si la teneur en NO est faible, l’ozone est consommé par la réaction. En plus de ces réactions, il existe d’autres voies secondaires de dégradation du CH4 (réaction avec le chlore atmosphérique et consommation par les bactéries méthanotrophes des sols).
Source
https://www.college-de-france.fr/site/e ... sphere.htmMais l'hydrogène réagit rapidement avec ·OH pour former de la vapeur d'eau et réduit donc la quantité de radicaux libres hydroxyles capables de dégrader le méthane dans la haute atmosphère.
Par ailleurs, l’augmentation du CH4 entraîne une diminution des radicaux ·OH et donc accroît la durée de vie du CH4.
L'hydrogène a le même effet.
Si on sature la capacité de production des radicaux ·OH par trop de méthane, le pourvoir réchauffant va augmenter puisque le méthane va rester lus longtemps dans l’atmosphère.